Jedną z najnowocześniejszych, skutecznych, bezpiecznych i bardzo komfortowych dla pacjenta form radioterapii jest brachyterapia z wykorzystaniem izotopowych stałych implantów, określana skrótem LDR-BT.
Brachyterapia LDR-BT
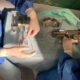
Implanty wykorzystywane w brachyterapii wszczepia się do tkanek lub narządów tam, gdzie zlokalizowany jest nowotwór lub bezpośrednio do guza. Po zakończonej terapii śródtkankowej pozostają one w ciele pacjenta do końca jego życia, bez aktywności promieniotwórczej.
Implanty stosowane w brachyterapii są maleńkie – ich długość to zaledwie kilka milimetrów, dlatego określa się je słowem ziarna. Tworzące je izotopy są źródłami energii o niskiej dawce mocy, ale ponieważ działanie implantu kumuluje się w dłuższym okresie czasu, dlatego też komórki guza docelowo otrzymują bardzo wysoką dawkę promieniowania. Przynosi to zamierzony efekt w postaci dokładnego niszczenia nowotworu, bez naruszenia narządów sąsiadujących. Ryzyko, że izotopowe „wszczepy” przemieszczą się po zakończeniu implantacji do innych tkanek, jest znikome, a zmniejszyło się znacznie od czasu, gdy wdrożono technikę łączenia poszczególnych ziaren cienkim łącznikiem z polimeru.
Stałe implanty w leczeniu nowotworów – jak to działa?
Najczęściej stałe implanty wykorzystuje się w leczeniu raka prostaty, ale znajdują też zastosowanie w terapiach innych nowotworów, m.in. w raku jamy ustnej czy piersi. Materiał śródtkankowy wytworzony jest z wyselekcjonowanego izotopu, który dobiera się w oparciu o unikalne dla każdego z nich parametry: wartość emitowanej energii i czas połowicznego rozpadu oraz pod kątem jego przeznaczenia. W brachyterapii z zastosowaniem stałych implantów wykorzystuje się izotopy jodu (I-125), palladu (P-103) oraz cezu (Cs-131). Mogą one być stosowane w monoterapii lub w terapiach łączonych, gdzie LDR-BT kojarzy się z napromienianiem guza wiązkami zewnętrznymi tak, aby uzyskać lepszy efekt leczniczy i wyższą dawkę końcową. Promieniowanie emitowane przez izotop tworzący implant doprowadza do niszczenia komórek nowotworowych w oparciu o mechanizmy analogiczne, które towarzyszą standardowej radioterapii.
Zanim implanty zostaną osadzone w ciele chorego, lekarz opracowuje plan leczenia i wyznacza docelowe usytuowanie materiału izotopowego. Samo wszczepianie implantów stałych przebiega w znieczuleniu ogólnym lub zewnątrzoponowym i pod kontrolą USG. Po zakończeniu procedury przeprowadza się badanie RTG, aby skontrolować lokalizację ziaren, oraz dozymetrię, czyli mierzy się parametry promieniowania. W ramach kontroli robi się tomografię komputerową i badania laboratoryjne w celu oszacowania wartości markerów charakterystycznych dla konkretnego nowotworu. Przy raku prostaty jest to głównie parametr PSA.
Pakiet nie tylko zdrowotnych korzyści
Mimo niewielkich rozmiarów, stałe implanty przynoszą chorym realne korzyści. Poprzez zastosowanie odpowiedniego izotopu i osadzenie materiału izotopowego dokładnie tam, gdzie promieniowanie powinno działać najsilniej, czyli w rejonie guza, do komórek nowotworowych dociera odpowiednio duża dawka leczniczego promieniowania, a jednocześnie uzyskuje się maksymalną ochronę zdrowych tkanek. Tak dobrego zabezpieczenia zdrowych tkanek przed napromienieniem nie da się osiągnąć w tradycyjnej radioterapii.
Brachyterapia w praktyce
Stałe implanty zwiększają szanse chorych na wyleczenie oraz skracają czas terapii i hospitalizacji związanej z samym zabiegiem implantacji w tkankach – bo często już następnego dnia po zabiegu brachyterapii pacjent wraca do domu. Zastosowanie LDR-BT zmniejsza też niebezpieczeństwo pojawienia się powikłań wynikających z samej terapii, co może mieć zasadnicze znaczenie dla jakości życia chorego – ocenianej krótko- i długookresowo. Przykładowo: wykorzystanie implantów stałych w leczeniu raka prostaty zmniejsza ryzyko wystąpienia takich powikłań, jak nietrzymanie moczu czy problemy z potencją.
Brachyterapia niską mocą dawki z wykorzystaniem stałych implantów jest bezpieczna – dla pacjenta i dla jego bliskich. Chory musi jednak pamiętać, aby przez okres 4-5 miesięcy po implantacji unikać bliskich kontaktów z małymi dziećmi (do 2 roku życia) i kobietami w ciąży.
W Polsce dostęp do terapii LDR-BT jest jeszcze ograniczony; mają go m.in. pacjenci Międzynarodowych Centrów Onkologii Affidea w Poznaniu.